Пн-Пт с 8:00 до 18:00 (Мск) без перерыва
- Разработка, производство и реализация диагностических наборов, контрольных материалов для клинической биохимии.
- Снабжение лечебных учреждений реактивами, расходными материалами и оборудованием.
- 01. Биохимические наборы реагентов
- 02. Контрольные материалы и калибраторы
- 03. Общеклинические исследования
- 04. Тест-полоски индикаторные
- 05. Коагулология, реагенты для исследования системы гемостаза
- 06. Сыворотки и диагностикумы
- 07. Цоликлоны, реагенты и принадлежности для определения групп крови
- 08. Системы для забора крови и принадлежности
- 09. Дозаторы и наконечники
- 10. Тесты, журналы, индикаторы и принадлежности для стерилизации
- 11. Питательные среды и растворы
- 12. Диски с антибиотиками, системы индикаторные для идентификации микроорганизмов
- 13. Красители для гематологии, цитохимии, микробиологии
- 14. Паразитология и микробиология
- 15. Микроскопы, масло иммерсионное и принадлежности
- 16. Лабораторное оборудование и расходные материалы
- 17. Реактивы для лабораторных исследований
- 18. Лабораторная посуда и изделия из пластмассы
- 19. Лабораторная посуда и изделия из стекла
- 20. Фарфоровая посуда и изделия из фарфора
- 21. Медицинские изделия из силикона и резины
- 22. Литература по лабораторной диагностике
-
Листовка "Биологические микроскопы торговой марки Микромед" (в формате pdf)

-
Листовка "Окраска по Цилю-Нильсену-100" (в формате pdf)

-
Листовка "Окраска микроорганизмов по Граму-100 (фуксин)" (в формате pdf)

-
Продукция собственного производства для клинической химии (в формате pdf)

-
Листовка "Лабораторная мебель за 15 дней" (в формате pdf)

-
Буклет на контрольную сыворотку Биоконт-С (в формате pdf)

Итоги негосударственной программы межлабораторного контроля качества определения гемоглобина (1993–1994 год.)
(Стендовый доклад на V Российском съезде специалистов по лабораторной диагностике, проходившем в Москве во Всероссийской Медицинской Академии Последипломного Образования 24–26 мая 1995 года.)
Программа была основана на добровольном и конфиденциальном участии. Цель Программы — обеспечение правильности и сопоставимости результатов определения гемоглобина и выявление возможных причин получения неправильных результатов.
Программа проводилась малым предприятием «Агат» при участии специалистов Гематологического Научного Центра РАМН. Время проведения — конец 1993 года — начало 1994 года.
1. Контрольный раствор гемоглобина «Биоконт-ГД»
(производства МП «Агат» ныне ООО «Агат-Мед»).
Контрольный раствор гемоглобина являются имитатором цельной крови и предназначен для проведения работ по контролю качества определения гемоглобина гемиглобинцианидным методом. Контрольный раствор гемоглобина представляет собой вязкую (соизмеримую по вязкости с кровью) жидкость от темно-красного до темно-коричневого цвета. Это водно-солевой раствор гемоглобина донорской крови, в качестве консерванта использован этиленгликоль в концентрации 30 об.%. Раствор очищен от стромальных примесей, что исключает ошибки, связанные с мутностью при спектрофотометрическом определении. Контрольные растворы гемоглобина устойчивы при длительном хранении при температуре +4° С. Допускается кратковременное хранение и транспортировка при температурах от -20 до +25° С.
2. Проведение программы
Каждому участнику были высланы контрольные материалы (3 флакона контрольного раствора гемоглобина «Биоконт-ГД» с различным, неизвестным для участников, содержанием гемоглобина в диапазоне концентраций от 70 до 180 г/л), инструкция по их применению, бланк протокола лабораторных измерений и специально разработанная анкета.
Истинная (аттестационная) концентрация контрольных растворов гемоглобина была определена гемиглобинцианидным методом в соответствии с рекомендациями Международного Комитета по Стандартизации в гематологии (ICSH) (ICSH Standard EP 6/2: 1977) тремя независимыми лаборантами на трех независимых приборах с общим коэффициентом вариации не превышающем 2 % и подтверждена в других лабораториях.
Участники программы должны были провести определение гемоглобина изо дня в день, в течение пяти дней, по одному разу из каждого флакона. Результаты полученных пятнадцати измерений, оформленные в виде протокола, и заполненные анкеты высылались в адрес МП «Агат» и обрабатывались статистическими методами.
Результаты программы (рассылались всем участникам) содержали следующие пункты: — общая неперсонофицированная оценка итогов программы (количество и структурный состав участников, итоговое отношение оценок качества работы); — индивидуальная оценка качества работы лаборатории и практические рекомендации.
3. Методика обработки данных
Общая (интегральная) оценка качества определения гемоглобина определялась как средний коэффициент вариации всех 15 определений по отношению к истинным концентрациям гемоглобина в образцах. Исходя из этой величины рассчитывался ранг (место) участника в общей совокупности. Полученные участником значения рассчитывались как средние из пяти определений для каждой концентрации.
Работу лаборанта оценивали как средний для трех концентраций коэффициент вариации относительно значений, полученных каждым участником.
Также полученные значения приводили к линейному уравнению вида:
Y = a0 + a1*X , относительно истинных значений.
Из него рассчитывали:
а0 — величину и ее достоверность отличия от 0 по критерию Стьюдента — выходит ли график из нулевой точки;
а1 — величину и достоверность ее отличия от 1 по критерию Стьюдента — завышает или занижает значения прибор, правильность калибровки;
— достоверность нелинейности показаний прибора — методом дисперсионного анализа по критерию Фишера.
4. Общие результаты программы
Всего в Программе приняло участие 182 лаборатории лечебных учреждений.
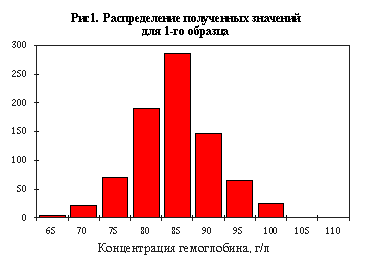
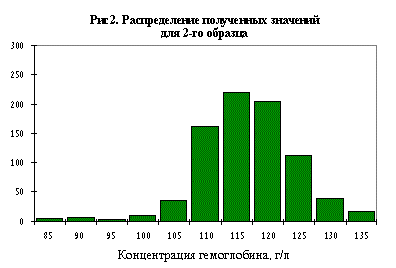
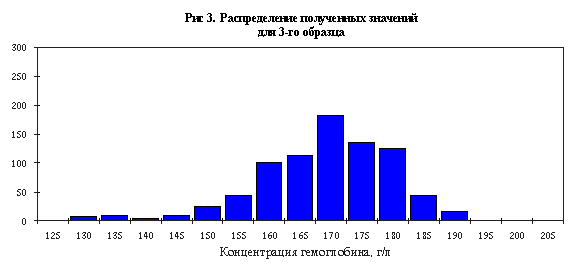
На рисунках 1, 2 и 3 показано распределение результатов, полученных для каждого образца.
![]()
![]()
![]()
![]()
Как видно из рисунков, полученные результаты измерений для каждого образца колебались в широких пределах. Так, для образца 2 диапазон полученных значений составил от 85 до 135 г/л.
Таблица 1
|
Номер образца |
Аттестационные значения, г/л |
Средние значения, определенные участниками, г/л |
Ошибка по отношению к истинной величине, %% |
|
1 |
83.18 + 0.28 |
82.7 |
- 0.6 |
|
2 |
119.61 + 0.39 |
114.8 |
- 4.1 |
|
3 |
174.08 + 0.39 |
167.3 |
- 3.9 |
В Таблице 1 представлены средние из полученных участниками значений. Судя по ним, можно предположить наличие общей систематической ошибке (занижении концентрации гемоглобина) в области высоких и средних значений.
5. Оценка полученных результатов
Допустимый предел аналитической вариации, принятый рабочей группой экспертов стран-членов СЭВ по научной разработке и унификации методов и средств клинической лабораторной диагностики для определения гемоглобина крови составляет 2%. По международным оценкам эта величина должна составлять не более 3%. В нашей программе средняя интегральная ошибка определения гемоглобина для всех участников составила 7.73%, что не может быть признано хорошим результатом. Достаточно условно мы разделили результаты на удовлетворительные (ошибка менее 4%) и неудовлетворительные. С ошибкой менее 4% программу выполнило 25% участников.
Для оценки качества работы лаборанта нами принята величина 2%, в этот интервал попало 60% участников.
Наиболее распространенная схема проведения программ контроля качества включает в себя использование двух образцов (высокой и низкой концентрации) и единичное определение концентрации компонента в образце. Качество работы лаборатории определяется по величине относительной ошибки измерений.
По CLIA (Федеральному Закону США) относительная ошибка измерения концентрации гемоглобина крови не должна превышать 7%.
На Рис.4 показано распределение относительных ошибок для всех полученных измерений. В 7% интервал попадает 1651 из 2442 измерений, что составляет 67.6%.
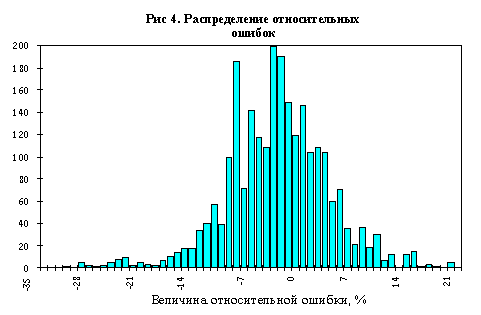

Наличие двух (и более) образцов в программе контроля качества позволяет определить причины возникающих ошибок по графику Юдена.
Пары значений для двух образцов от каждого участника наносят в виде точек на график. Если точки попали внутрь окружности, результаты пригодны. Если точки располагаются вне окружности, но между параллельными прямыми, это значит, что лаборатории получили завышенные или заниженные величины для обеих проб и что имеются систематические ошибки. Точки, близкие к диагонали, показывают, что лаборатории работают стабильно. Точки, попавшие в другие секции графика свойственны случайным ошибкам. На рис. 6 приведен график Юдена для пары 2—3 образца. Отложена величина процента ошибки для среднего значения, полученного в каждой лаборатории.
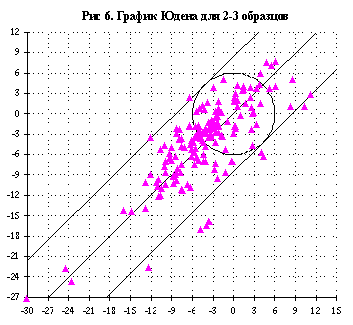
Можно отметить высокую стабильность работы лабораторий, малое число случайных ошибок, линейность измерений в интервале средних-высоких концентраций гемоглобина. При этом наблюдается значительная систематическая ошибка (чаще в сторону занижения результата), что приводит к низкому общему уровню качества определения гемоглобина.
6. Анализ причин ошибок в определении концентрации гемоглобина
6.1. Для анализа возможных причин ошибок
в определении концентрации гемоглобина каждый участник, помимо контрольных образцов, получил, заполнил и отправил организатору анкету, содержащую следующие вопросы:
Вопросы для заведующего клинической лабораторией:
1. При какой организации состоит Ваша клиническая лаборатория? Для больниц, госпиталей указать число коек. Для поликлиник указать количество человек, прикрепленных для обслуживания.
2. Принимала ли Ваша лаборатория участие в программах межлабораторного контроля качества определения гемоглобина ? Если «да», указать: когда (год), кто проводил программу.
3. Есть ли у Вас система внутрилабораторного контроля качества определения гемоглобина? Если «да», указать: — как часто и по какой программе проводится контроль качества (ежедневно, периодически, иногда, используя метод контрольных карт, др.); — какие контрольные материалы используются название фирма-производитель.
4. Общее число персонала, работающего в клинической лаборатории.
5. База обучения лаборанта, определяющего гемоглобин.
6. Стаж его работы с методом.
7. Время от начала анализа до выдачи результата.
Вопросы для лаборанта:
1. Характеристика прибора (марка).
2. Используемый набор реактивов название, фирма-производитель, срок годности.
3. Калибровка прибора: — по стандарту, прилагаемому к набору; — по другому стандарту, если «да», указать: фирма-производитель, срок годности; — другим способом (указать).
4. Время инкубации пробы (мин).
Статистически сопоставляя полученные данные анкет и результатов измерений нам удалось выделить несколько факторов, влияющих на качество определения гемоглобина. Приведенные в дальнейшем цифры имеют (если не оговорено особо) достоверность различий не менее 9%.
6.2. Наличие системы внутрилабораторного контроля качества определения гемоглобина:
такую систему контроля в том или ином виде имеют 84% участников программы.
В качестве контрольного материала лаборатории используют:
— контрольные материалы собственного производства, гемолизаты и сливную кровь — 26 лабораторий (18% от числа проводящих контроль);
— стандартные образцы цианметгемоглобина, отдельные и входящие в состав наборов — 31 лаборатория (22%);
— контрольные растворы гемоглобина промышленного производства — 74 лаборатории (52%), в том числе 66 лабораторий (47%) используют контрольные материалы «Биоконт-ГД» и «Биоконт-ГД-Н» производства МП «Агат».
Средние интегральные ошибки определения гемоглобина для этих групп составляют:
— без регулярного контроля качества — 8.62%;
— с применением для контроля стандартных образцов цианметгемоглобина — 7.54%;
— с использованием материалов собственного производства — 10.48%;
— с использованием контрольных растворов гемоглобина промышленного производства — 6.37%.
Регулярное проведение контроля качества оказывает влияние и на качество работы лаборанта. Так, при его отсутствии средний коэффициент вариации в серии составляет 2.68 %, а с ним — 2.37%. При этом качество определений не зависит от стажа работы лаборанта.
Таким образом, проведение внутрилабораторного контроля оказывает заметное влияние на качество работы лаборатории, однако для его эффективного использования решающую роль играет характер используемого контрольного материала. В качестве наилучшего может быть рекомендован контрольный раствор гемоглобина с использованием этиленгликоля в качестве консерванта, промышленного производства (типа «Биоконт-ГД»).
6.3. Участие в программах внешнего контроля
В программах внешнего контроля качества, проводимых, как правило, региональными центрами клинической диагностики, принимали участие 41% участников нашей программы. Для этой группы, по сравнению с теми, кто в таких программах не участвовал, получены следующие цифры: 7.57% против 7.83% для общей ошибки и 1.97% против 2.69% для ошибки работы лаборанта.
6.4. Используемые методы и приборы
В Таблице 2 приведено распределение участников по используемым ими методам определения гемоглобина, общие ошибки для каждой группы (для этих значений оценка достоверности различий не проводилась), а также количество и процент приборов внутри группы, имеющих нелинейную характеристику. Прибор считался нелинейным, если достоверность нелинейности по критерию Фишера превышала 95 % и общая ошибка измерений превышала 3 %.
Подавляющее большинство используют в своей работе гемиглобинцианидный метод и наборы для его проведения следующих предприятий: Екатеринбургского предприятия по производству бактериальных препаратов, НПО «Биолар», «Ремикс» (Уфа), «Синтакон» (Санкт-Петербург).
Четыре участника используют аммиачный метод (двое уточнили, что по Дервизу и Воробъеву), и хотя мы не можем рекомендовать этот метод, так как он содержит предпосылки систематических ошибок, превышающих должный уровень точности, на существующем фоне они не оказывают заметного влияния. Один участник использует метод Сали, и в этом случае ошибка чрезвычайно велика.
Таблица 2
|
Методы и приборы |
Общее количество |
Общая ошибка, %% |
Нелинейность приборов |
Количество % от группы |
|
Все участники |
169 |
7.73 |
65 |
38.5 |
|
Гемиглобинцианидный метод |
160 |
7.56 |
61 |
38.1 |
|
В том числе на приборах |
|
|
|
|
|
КФК-2 |
87 |
7.58 |
30 |
34.5 |
|
КФК-3 |
25 |
6.70 |
12 |
48.0 |
|
МФ-1020 |
16 |
8.26 |
7 |
43.8 |
|
КФО |
5 |
6.95 |
3 |
60.0 |
|
Гемокон-5 |
3 |
6.73 |
1 |
33.3 |
|
ФЭК-56 |
6 |
5.29 |
2 |
33.3 |
|
ГФ-3 |
3 |
4.48 |
1 |
33.3 |
|
6 |
4 |
12.06 |
3 |
50.0 |
|
Аммиачный метод |
4 |
7.59 |
- |
- |
|
Метод Сали |
1 |
21.9 |
- |
- |
|
Импортные приборы |
6 |
3.64 |
0 |
0.0 |
В качестве приборной базы используют различные фотоколориметры. Разброс средних общих ошибок для различных типов приборов позволяет предположить значительный вклад ошибки прибора в общую точность измерений.
Обращает на себя внимание большое количество приборов с существенной нелинейностью характеристики, причем для всех типов приборов. Особенно выделяется в этом ряду гемоглобинометр ГФ-Ц-4.
Особо надо отметить сравнительно небольшую группу лабораторий, которые имеют импортные приборы : «Stat-LAB», «Celltac» (Япония), «Contraves Digicell — 500» (Швеция), «Serono — 150» (Serono), T-840 «Культер» (Культроник, Франция), «KSMA» (даны в орфографии участников). Для этой группы общая ошибка составляет 3.64 %; ошибка работы лаборанта — 1.30 %; характеристика всех импортных приборов носит линейный характер.
7. Репрезентативность выборки и оценка результатов
Сравнительно небольшое (по отношению к общему числу существующих клинических лабораторий) количество участников и неслучайность сложившейся выборки не позволяет нам однозначно сопоставить полученные результаты с истинным положением дел по определению гемоглобина в стране.
Тем не менее, можно предположить некоторые тенденции, а именно: рассылка приглашений на проведение программы контроля качества была осуществлена по адресам базы данных МП «Агат», в том числе и его постоянным клиентам (МП «Агат» специализируется на производстве контрольных материалов для клинической биохимии, в том числе и на производстве контрольных растворов гемоглобина — торговая марка «Биоконт»). Поэтому значительное количество участников использует в своей работе по внутреннему контролю качества продукцию этого предприятия.
Всего было разослано более 3000 приглашений, на которые откликнулись всего около двухсот лабораторий (некоторые не выслали потом результатов или выслали их поздно, для того чтобы войти в общий статистический анализ). Можно предположить, что участие в программе приняли учреждения, уделяющие особое внимание работе над контролем качества лабораторных исследований и использующие для этого каждую возможность.
Выше мы показали, что участие в программах внешнего контроля, не будучи связано напрямую, коррелирует с качеством работы лаборатории, так как является отражением общего профессионального уровня ее сотрудников. Таким образом, вероятно, качество определения гемоглобина в клинических лабораториях в целом по стране ниже, и заметно, чем полученные нами результаты.
8. Стоимость программы
Данная программа проводилась на коммерческой основе, участники программы вносили по 3 тыс. рублей (на начало 1994 г). Однако реальная стоимость программы оказалась выше (большую часть стоимости составляют почтовые и полиграфические расходы). По нашим оценкам стоимость таких программ на настоящее время не должна превышать 50 тысяч рублей на одного участника.
9. Выводы и рекомендации
Определение концентрации гемоглобина в крови является одним из наиболее распространенных клинических лабораторных анализов. Однако диапазон изменений концентрации гемоглобина при патологии сравнительно невелик относительно нормальных значений, что диктует жесткие пределы ошибок при измерениях, более жесткие, чем при определении большинства других биохимических параметров.
Проведенная нами программа внешнего контроля качества определения гемоглобина показала, что качество проведения этого анализа во многих лечебных учреждениях является неудовлетворительным.
Большой объем программы (три образца по пять измерений) позволил расчленить общую ошибку и оценить вклад отдельных ее составляющих. Так, точность работы лаборантов (сюда входят точность пипетирования трансформирующего раствора и образца крови, полнота перемешивания, достаточное и постоянное время проведения реакции а также точность гематологических капилляров) оказалась в целом удовлетворительной. С другой стороны, частая нелинейность используемых приборов, которые калибруются как правило по одной точке, может приводить к значительным ошибкам при определении концентраций, отличных от концентрации калибратора. Анализ графиков Юдена также показывает основное влияние не случайных, а систематических ошибки.
Частично исправить положение может использование систем внутреннего контроля качества, однако для эффективности таких программ необходимо использование в них специальных контрольных материалов — контрольных растворов гемоглобина промышленного производства с точно известными и постоянными во времени значениями концентраций (типа «Биоконт-ГД»).

- Биохимические наборы реагентов
- Контрольные материалы и калибраторы
- Красители для гематологии, цитохимии, микробиологии
- Микроскопы, масло иммерсионное и принадлежности
-
Контрольная сыворотка Биоконт-С
-
Масло иммерсионное
-
ГЕМОГЛОБИН-КОНТРОЛЬ


